⚛️Disoluciones y diluciones: teoría fácil, ejercicios y vídeos resueltos⚗️⚗️
Moles, molaridad lo que se conserva y lo que cambia en los problemas
Índice del post:
- Lo que debes entender antes de resolver ejercicios de disoluciones y diluciones
- Videoclase con las ideas clave para no liarte 🎥
- Infografía descargable gratis con las fórmulas esenciales
- 20 ejercicios para practicar disoluciones y diluciones
- Resolución en vídeo de los 20 ejercicios por 6 € (en oferta por 3 meses)🎥
Lo que cambia y lo que se conserva
Hoy toca uno de esos temas que parecen un lío… hasta que entiendes dos ideas clave: disoluciones y diluciones.
Y te lo digo de verdad: gran parte de los problemas de este tema no fallan por química, fallan porque no se entiende bien qué representa la concentración, qué cambia y qué se conserva.
Cuando eso se ve claro, casi todo se convierte en reglas de tres con sentido.
Antes de lanzarte a los vídeos, quiero que te quedes con unas cuantas ideas que te van a ahorrar muchísimos errores.
La primera es esta: la concentración no depende de que tengas mucha o poca cantidad de disolución, sino de la proporción entre soluto y disolución.
Qué es la concentración y por qué no depende del volumen total
Piensa en una taza de café o de cola-cao. Si te gusta más cargado, tendrá un color más oscuro; si te gusta más suave, será más claro. Ahora imagina que coges una cucharada de esa taza. ¿Cambia el color por coger menos cantidad? No. Sigue igual de oscuro. ¿Por qué? Porque la concentración es la misma.
Eso es exactamente lo que pasa en química.
Puedes tener:
- 10 mL de una disolución 0,5 M
- 2 L de una disolución 0,5 M
Y ambas tienen la misma concentración.
Entonces, ¿qué cambia?
Cambia la cantidad total de sustancia que tienes. En química, eso normalmente lo medimos en moles.
Por ejemplo, si una disolución tiene concentración 0,1 M, eso significa que en 1 L hay 0,1 moles. Si en vez de 1 L tomas solo 10 mL, la concentración sigue siendo 0,1 M, pero la cantidad de sustancia que has cogido es menor.
Esta idea es clave:
menos volumen no significa menos concentración; significa menos cantidad total de soluto.
Qué se conserva en una dilución y qué cambia
La segunda idea importante es la que manda en las diluciones: al diluir, los moles de soluto se conservan.
¿Por qué? Porque en una dilución no añades más soluto ni quitas soluto. Lo único que haces es añadir disolvente, normalmente agua.
Volvamos al café. Coges una cucharada de café de una taza. Esa cucharada tiene la misma concentración que la taza entera, aunque tenga menos cantidad. Ahora le añades leche o agua. ¿Qué pasa? Que el color se aclara. Está más diluido. Pero el café no ha desaparecido. Sigue habiendo la misma cantidad de café que había en la cucharada del principio; simplemente ahora está más repartido en más volumen.
Eso es una dilución.
Así que, en una dilución:
- los moles de soluto se mantienen
- el volumen aumenta
- la concentración disminuye
Este es, probablemente, el error más frecuente: pensar que al añadir agua “se pierde” soluto.
No se pierde nada. El soluto sigue ahí. Solo está más disperso.
Moles y molaridad: la diferencia que evita muchos errores
Otra idea que tienes que separar bien es esta: moles no es lo mismo que molaridad.
- Los moles te dicen cuánta sustancia hay.
- La molaridad te dice cuánta sustancia hay por litro de disolución.
Por eso:
- si tienes los mismos moles en más volumen, la molaridad baja
- si tienes los mismos moles en menos volumen, la molaridad sube
Ahora vamos a lo que suele pasar en los ejercicios.
Si preparas una disolución a partir de un sólido, normalmente el camino es:
- calcular cuántos moles necesitas
- pasar esos moles a gramos
- preparar el volumen final que te piden
Si haces una dilución, recuerda siempre esto:
- los moles iniciales y finales del soluto son los mismos
- el volumen que tomas de la disolución no es el volumen final
- “enrasar hasta 250 mL” significa que el volumen final de la disolución será 250 mL, no que añades 250 mL de agua
Si mezclas dos disoluciones, tampoco vale hacer la media de concentraciones sin más. Primero tienes que calcular cuántos moles aporta cada una, sumarlos y después dividir entre el volumen final.
Y una última advertencia, porque aquí también cae muchísima gente:
más volumen no significa más concentración.
Puede significar que tienes más cantidad total de soluto, sí. Pero la concentración solo depende de la relación entre la cantidad de soluto y el volumen total de disolución.
Cuando entiendes todo esto, los problemas dejan de parecer fórmulas sueltas y empiezan a tener lógica.
Quédate con este resumen:
- la concentración es una proporción
- no depende de tener mucho o poco volumen
- en las diluciones se conservan los moles de soluto
- al añadir agua, la concentración baja, pero el soluto no desaparece
- antes de calcular, entiende qué está pasando físicamente
Con esa base, la mayoría de problemas de disoluciones y diluciones se vuelven mucho más fáciles.
Cómo enfocar los problemas de disoluciones y diluciones sin liarte
Infografía descargable gratis con todas las fórmulas
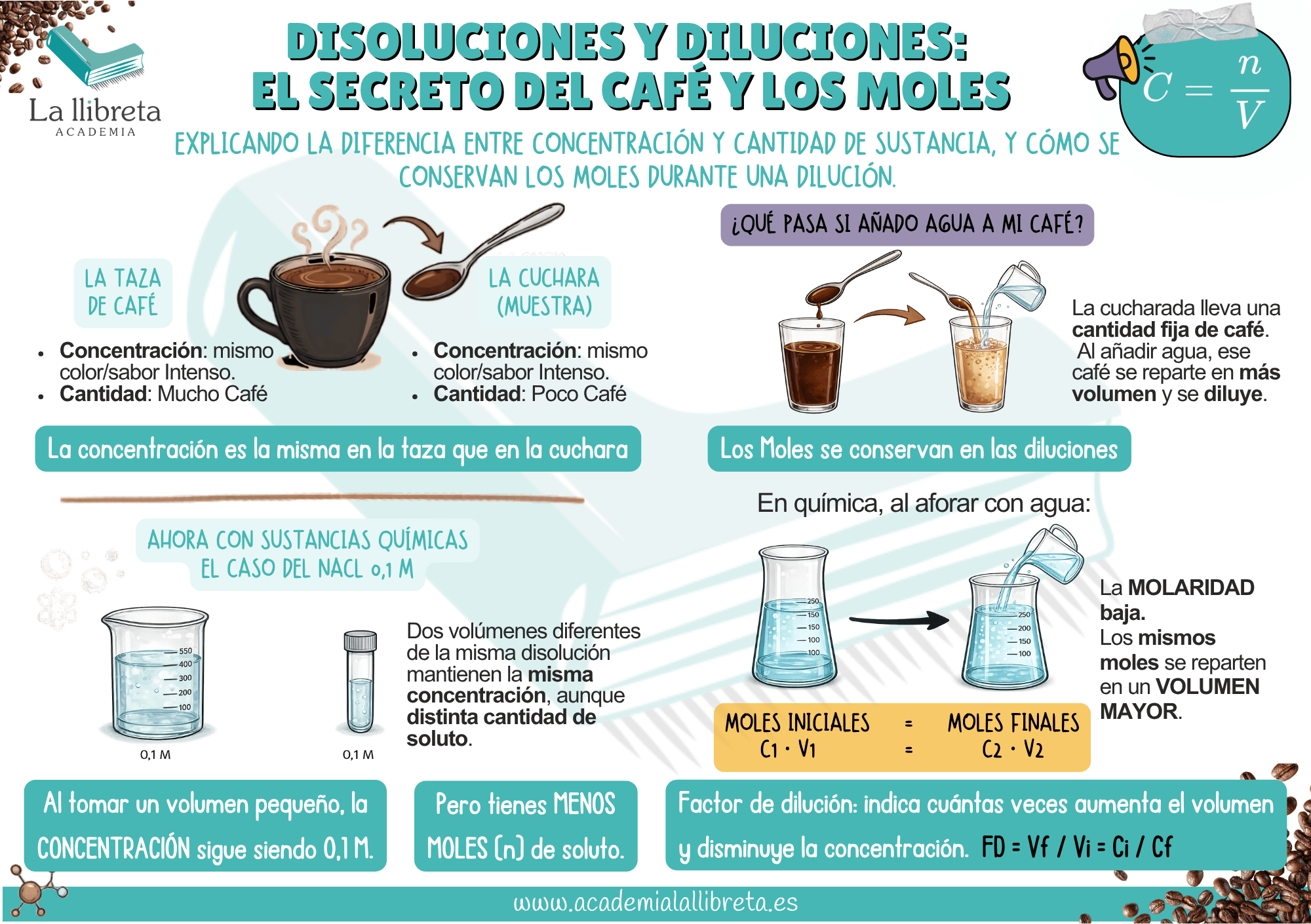
Descarga gratuita – Infografía disoluciones y colección de problemas
20 problemas para practicar disoluciones y diluciones
¡Ahora te toca a ti!
Ahora toca demostrar que lo has entendido de verdad.
Te dejamos una serie de ejercicios sobre disoluciones, diluciones, moles, molaridad y otras formas de expresar la concentración para que practiques como toca: haciendo problemas.
Primero, inténtalos por tu cuenta.
Después, comprueba el resultado con nuestras resoluciones en vídeo.
Tienes algunos vídeos gratis para empezar. Y, si quieres acceder al resto, puedes desbloquearlos por solo 6 € (en oferta por 3 meses)
Puede parecer un precio pequeño, pero detrás hay algo grande: horas de profes preparando materiales, seleccionando ejercicios, grabando explicaciones y buscando la forma más clara de ayudarte a entender lo que en clase muchas veces se atraganta.
En La Llibreta no hacemos contenido por rellenar. Lo hacemos para que entiendas, ganes seguridad y avances de verdad.
Si puedes apoyarnos, ese pequeño pago nos ayuda a seguir creando recursos útiles, claros y cercanos.
Y a ti te da acceso a un material pensado para ponértelo más fácil.
Haz los gratuitos, comprueba cómo te ayudan y, si te encaja nuestra forma de explicar, por 6 € tienes el resto (oferta de 3 meses).
🎯 Conclusión: ¿Te ha resultado útil este post?
Esperamos que esta selección de problemas clave de redox te haya ayudado a comprender mejor este tema fundamental para la PAU y la PCE. Sabemos que algunos ejercicios pueden ser un reto, pero con práctica y una buena estrategia, nada te pillará por sorpresa en el examen.
📌 Ahora cuéntanos: ¿Te ha sido útil esta guía?
💬 Déjanos un comentario con tus impresiones o dudas, nos encanta saber cómo podemos seguir ayudándote.
⭐ Si te ha gustado, apóyanos con una reseña en Google, ¡eso nos motiva a seguir creando contenido de calidad para ti! 🚀
📺 ¿Quieres más problemas resueltos?
No olvides visitar nuestro blog y nuestro canal, donde seguimos subiendo vídeos explicativos, trucos y estrategias para que llegues al examen con total confianza.
🔗 Sigue aprendiendo aquí: más recursos de química
¡Mucho ánimo con tu preparación y a por ese 10 en química! 💪⚛️
🧪 PRÉPARATE EN LA LLIBRETA
En La Llibreta, ofrecemos una variedad de cursos que se adaptan a tus necesidades, tanto en formato presencial como online. Además de nuestras clases en directo, contamos con cursos online en diferido que incluyen video clases detalladas, exámenes resueltos, resúmenes, y cuestionarios autocorregibles, entre otros recursos. También tienes la opción de comprar solo el material didáctico, sin incluir las videoclases.
🎓 ¿Por qué nuestros materiales son una herramienta imprescindible?
- Diseñados por Docentes Expert@s:
Creados por profesor@s que conocen a fondo los exámenes y han seleccionado y organizado toda la información relevante para que te prepares con confianza. - Visuales, Memorables y Complejos:
Nuestros apuntes, esquemas y ejercicios están diseñados con un enfoque visual para facilitar la comprensión y la memorización, ideal tanto para estudiar en profundidad como para una rápida revisión antes del examen. - Contenido Completo y Conciso: Resúmenes claros, ejercicios resueltos y esquemas organizados en un formato fácil de manejar. Todo lo que necesitas para estudiar de manera eficiente está resumido en un solo lugar.
- Ejercicios y Exámenes Resueltos: Incluimos ejercicios interactivos, exámenes de convocatorias anteriores resueltos y organizados por bloques. Practica y refuerza lo aprendido de manera práctica y efectiva.
- Esquemas Aclaratorios: Esquemas que simplifican los conceptos más complejos, permitiéndote comprender y repasar con mayor facilidad.
Química PAU: elige tu pack y empieza hoy
Desde 20 € · acceso inmediato · material actualizado a la última convocatoria
-
Exámenes (20 €)
-
Apuntes Plus (40 €)
-
Vídeo Cursos (99 €)
-
PAU 360º (99 € + 20 €/mes)
¿Clases en directo o particulares? Haz clic aquí.
Matrícula abierta 2026–2027
Reserva tu plaza para el nuevo curso
Matrícula abierta 2026-2027
¡Apúntate al curso anual PAU 2027!
Prepárate en la Llibreta
Prepárate con nuestroscursos híbridos. Podrás asistir de manera presencial u online. ¡Además las clases se quedan grabadas!
Compra nuestros apuntes
Tienes nuestros apuntes, esquemas, resúmens, glosarios y mucho más disponibles por 40€ y el curso de videomaterial por 190€.
Exámenes de química
Todos los exámenes de Química RESUELTOS de la EVAU, PCE, PAU+25 y PAGS
Más recursos de química
Calculadora de notas
Utiliza nuestro simulador de notas y descubre cuál es tu objetivo para que te alcance la nota de corte.
También te puede interesar
Polímeros en Selectividad y PCE: la parte de Química que parece fácil… hasta que cae en el examen
Guía rápida sobre polímeros en Química para Selectividad, PAU y PCE: adición, condensación, tipos, ejemplos y trampas típicas de examen.
Problemas redox de la PAU y PCE que debes saber resolver
Si te preparas para la PAU o la PCE, estos problemas de redox son imprescindibles. Descubre errores tipo y saca un 10.
Redox para PAU y PCE: Resumen, Trucos y Ajuste
Domina redox en la PAU y PCE con nuestros consejos y trucos para resolver problemas complejos y comunes en Selectividad.
Aprende a resolver problemas de estequiometría paso a paso
🧪 Cómo empezar un problema de estequiometría (sin perderte) 🌟 La guía definitiva para convertir cualquier dato en moles y resolver tus ejercicios con éxito Índice del post: 🎥 Videoclase de introducción a la estequiometría 📘 Explicación paso a paso 🧠 Infografía...
Ejercicios de Estequiometría: Test Online para Entender Moles, RL y Disoluciones
🧪 Ejercicios de Estequiometría para Pensar (y Entender de Verdad la Química) 🌟 Practica la estequiometría con ejercicios autocorregibles, explicaciones claras y tests diseñados para que aprendas razonandoEste post no es solo teoría: es un campo de prácticas de...
Ajustar reacciones químicas nunca había sido tan fácil
Aprende a ajustar reacciones químicas sin miedo Aprende con explicaciones claras y ejercicios interactivos pensados para ayudarte de verdadHola, Hoy queremos ayudaros a dominar el ajuste de reacciones químicas. Sabemos que para muchos/as estudiantes que empiezan con...
Problemas de ácido base en PAU y PCE que tienes que saber resolver
Si te preparas para la PAU o la PCE, estos problemas de ácido base son imprescindibles. Descubre errores tipo y saca un 10.
Ácido-Base para PAU y PCE: Resumen, Trucos y Problemas Resueltos
Domina el equilibrio químico PAU PCE con nuestros consejos y trucos para resolver problemas complejos y comunes en Selectividad.
Equilibrio Químico para PAU y PCE: Resumen, Trucos y Problemas Resueltos
Domina el equilibrio químico PAU PCE con nuestros consejos y trucos para resolver problemas complejos y comunes en Selectividad.
Problemas de equilibrio químico en PAU y PCE que debes saber resolver
Si te preparas para la PAU o la PCE, estos problemas de equilibrio químico son imprescindibles. Descubre errores tipo y saca un 10.

