⚛️Reacciones Redox: Resumen, Trucos y Guía de Supervivencia para PAU y PCE⚗️
Domina el ajuste ión-electrón, las pilas y la electrólisis con los trucos definitivos para no fallar en tus exámenes de Química
¡Hola a tod@s! Hoy nos sumergimos en uno de los temas estrella de Química para PAU y PCE: las reacciones de oxidación-reducción (Redox). También se conocen como reacciones de transferencia electrónica, ya que en ellas siempre hay un intercambio de electrones: una sustancia se comporta como reductor (los pierde) y otra como oxidante (los gana). Es un concepto muy similar al de las reacciones ácido-base donde se intercambiaban protones, ¡pero ahora los protagonistas son los electrones!
1. ¿Qué es una reacción Redox? Conceptos Clave
Lo primero es no hacerse un lío con los nombres. En una reacción Redox, siempre hay alguien que «da» y alguien que «recibe»:
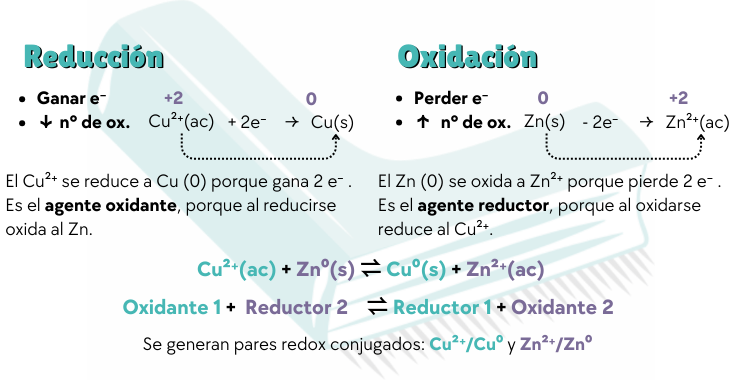
- Oxidación: Es perder electrones (e−). El número de oxidación sube.
- Reducción: Es ganar electrones (e−). El número de oxidación baja.
👀 Truco para no fallar: ¡Los nombres van al revés!
- El que se reduce es el agente oxidante (porque provoca la oxidación del otro).
- El que se oxida es el agente reductor (porque provoca la reducción del otro).
Los Pares Redox Conjugados
Para entender bien una reacción química redox, debemos verla como un proceso donde una sustancia se comporta como oxidante y otra como reductor de forma simultánea. Esto genera lo que llamamos pares redox conjugados, que siguen este esquema general:
Oxidante₁ + Reductor₂ ⇌ Reductor₁ + Oxidante₂
Un ejemplo clásico que verás en tus exámenes es la reacción entre el Cobre y el Zinc: Cu²⁺(ac) + Zn⁰(s) ⇌ Cu⁰(s) + Zn²⁺(ac)
En esta reacción identificamos dos parejas o pares: Cu²⁺/Cu⁰ y Zn²⁺/Zn⁰.
El Cu²⁺ gana 2 e− para convertirse en Cu⁰, por lo que se reduce y actúa como el agente oxidante (ya que provoca la oxidación del Zinc).
El Zn⁰ pierde 2 e− para convertirse en Zn²⁺, por lo que se oxida y actúa como el agente reductor (provocando la reducción del Cobre).
👀 Truco de La Llibreta: Para identificar los pares rápidamente, busca siempre el «antes» y el «después» de cada elemento en la ecuación. Recuerda que no puede haber una oxidación sin una reducción y viceversa. Si identificas quién gana electrones, automáticamente habrás encontrado al agente oxidante y su par conjugado será la forma reducida del mismo elemento.
2. Los Números de Oxidación: La base de todo
No puedes ajustar una reacción si no sabes los números de oxidación. Aquí te dejamos las reglas de oro:
- Elementos libres (Cu, O₂): Siempre 0.
- Oxígeno: Normalmente -2, excepto en peróxidos (H₂O₂) que es -1 y cuando se combina con F que es +.
- Hidrógeno: +1 en ácidos (con no metales) y -1 en hidruros metálicos.
- Iones: La suma de los números de oxidación debe dar como resultado la carga del ión.
🎥 Vídeo recomendado: Si todavía te bailan los números, echa un vistazo a este vídeo donde calculamos números de oxidación paso a paso.
Vídeo extraído de la plataforma de Academia La Llibreta. Compra las videoclases aquí: cursos online La llibreta.
👀 Truco de La Llibreta:
Para saber la carga de un ión poliatómico, fíjate en su ácido de procedencia. Los protones siempre actúan con +1; por tanto, si el H₂SO₄ tiene 2 hidrógenos, el grupo SO₄ tiene que tener una carga de SO₄²⁻.
¡Conocer los oxoácidos más comunes te permitirá saber la carga del anión al instante!
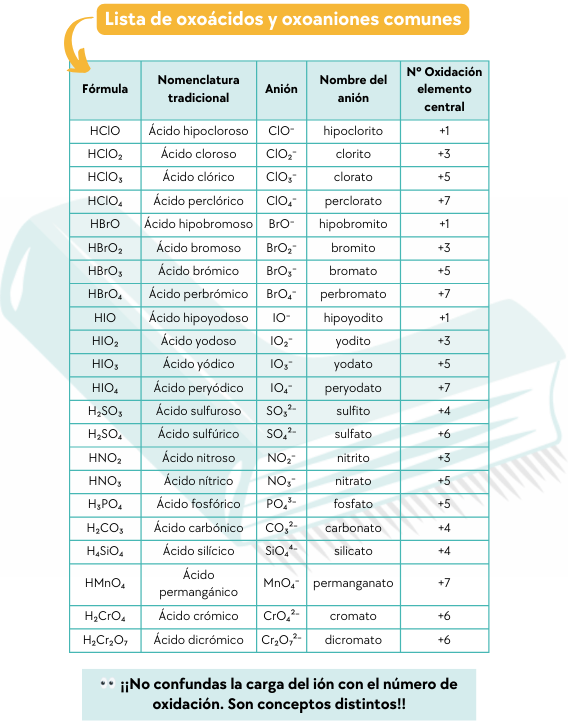
🔗 Post relacionado: [Aprende a disociar y conoce los iones comunes aquí]
3. Ajuste por el Método del Ión-Electrón
3.1 Ajuste en medio ácido
Si intentas ajustar una reacción redox por tanteo te puede dar dolor de cabeza, lo puedes conseguir, pero como entran en juego otros conceptos y además te lo exigen en el examen, mejor que aprendas este método.
Es importante no saltarse ningún paso y hacer comprobaciones, porque cometer errores es muy fácil:
- Escribir la ecuación redox en su forma iónica sin ajustar: Se disocian ácidos, hidróxidos y sales para formar la ecuación iónica básica, sin ajuste de masas.
- Asignar números de oxidación y determinar qué especies se reducen y cuáles se oxidan.
- Escribir las semirreacciones de oxidación y reducción: Se recomienda mantener un orden constante, por ejemplo, escribir primero la semirreacción de reducción y luego la de oxidación. Esto ayuda visualmente a recordar dónde se añaden los electrones (e⁻).
- Ajustar masas si es necesario (👀 ojo, no ajustar las masas es un error muy común)
- Balance de oxígeno: Añadir moléculas de agua (H₂O) para compensar la diferencia de oxígenos.
- Balance de hidrógenos: Añadir protones (H⁺) al lado que carezca de hidrógenos. Es crucial contar con todos los hidrógenos presentes (👀ojo con NH₃, H₂O₂ que ya tienen H)
- Balance de carga: Se añaden e⁻ para equilibrar las cargas, prestando atención a los cambios en los números de oxidación. Es aconsejable verificar este paso de dos maneras distintas:
- Observar los cambios en los números de oxidación y calcular la ganancia o pérdida de e⁻.
- Calcular el número de cargas iónicas en ambos lados y añadir e⁻ para igualar las cargas.
- Debe coincidir el º de e⁻ en ambos casos.
- Multiplicar las semirreacciones por los factores adecuados para igualar el número de e⁻ entre ellas.
- Sumar las semirreacciones y cancelar los e⁻ resultantes para obtener la ecuación iónica ajustada.
- A partir de la ecuación iónica ajustada, escribir la ecuación molecular ajustada.
- 👀Ojo puede haber alguna especie que se ajuste por tanteo y que no aparezca en las semirreacciones.
- 👀 Ojo con moléculas como el H₂SO₄ si tienes 3 H⁺ se ajustará con 3/2 H₂SO₄.
- COMPROBAR: Debe de haber el mismo número de átomos a ambos lados de la ecuación química. En caso contrario debes buscar el error.
🎥 Problema Resuelto en vídeo: Aquí tenéis un vídeo con un ajuste completo en medio ácido para que veáis cómo se aplican todos estos pasos.
3.1. Ajuste en Medio Básico
Si el examen te pide ajustar en medio básico, el procedimiento es prácticamente idéntico al anterior, con una excepción crucial en el paso 3 (el balance de O e H):
- Balance de oxígeno: Añade moléculas de agua (H₂O) en el lado donde sobren oxígenos.
- Balance de hidrógenos: Añade grupos hidróxido (OH⁻) en el lado contrario.
👀 Truco de La Llibreta: Muchos/as estudiantes se confunden porque en medio ácido el agua se pone donde faltan oxígenos, pero en básico es al revés (donde sobran). Un buen método para comprobar que vas bien es verificar que, tras añadir los OH⁻, la carga total y el número de átomos cuadren perfectamente.
3.2. Casos Especiales: Peróxidos (H₂O₂)
Los peróxidos, como el peróxido de hidrógeno, suelen ser el «punto flaco» de muchos estudiantes porque el oxígeno no actúa con su número habitual.
Regra de oro: En los peróxidos, el número de oxidación del oxígeno es -1.
La dificultad: A veces es difícil identificar el cambio porque en la misma reacción puede haber otros oxígenos que sí actúan con -2.
Normalmente, el peróxido de hidrógeno cambia a H₂O (reducción) o a O₂ (oxidación) siguiendo estas semirreacciones:
- Reducción: H₂O₂ + 2H⁺ + 2e⁻ → 2H₂O
- Oxidación: H₂O₂ → O₂ + 2H⁺ + 2e⁻
👀 ¡Ojo con los Hidrógenos! Al ajustar las masas, no olvides que el H₂O₂ ya contiene hidrógenos en su molécula. Tenlo en cuenta antes de empezar a añadir protones (H⁺) a lo loco para que el balance final sea correcto.
4. Pilas Electroquímicas (Celdas Galvánicas)
Las pilas electroquímicas son dispositivos diseñados para transformar la energía química en energía eléctrica de forma espontánea. Funcionan separando las dos semirreacciones de una reacción redox en compartimentos distintos, obligando a los electrones a viajar por un circuito externo.
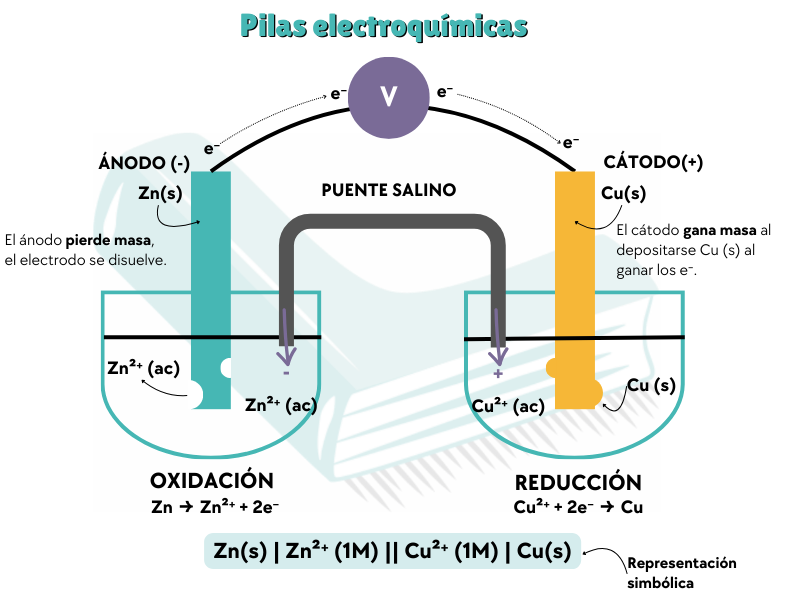
👀 A tener en cuenta:
- Dónde ocurren las semirreacciones:
- Ánodo (-): Es el polo donde ocurre la oxidación. Actúa como fuente de electrones y, al perder material, el electrodo pierde masa y se disuelve.
- Cátodo (+): Es el polo donde ocurre la reducción. Los electrones (e⁻) llegan aquí y son ganados por los cationes en disolución, haciendo que el electrodo gane masa al depositarse el metal.
- Fuerza Electromotriz (FEM): La FEM o potencial de la pila (E) indica la diferencia de potencial eléctrico entre el ánodo y el cátodo, midiéndose siempre en voltios (V).
- Potenciales de Referencia Estándar: Para medir potenciales de forma comparable, se usan condiciones estándar: concentración 1 M, temperatura de 25 °C y presión de 1 atm. Se utiliza como referencia universal el potencial estándar del hidrógeno: Eº (2H⁺/H₂) = 0 V.
- Dirección de los Potenciales: En los libros y exámenes, los potenciales están tabulados como reducción. Si necesitas el proceso inverso (oxidación), simplemente inviertes la reacción y cambias el signo del potencial.
- Poder Oxidante: Cuanto mayor sea el potencial de reducción (más positivo), mayor es la tendencia de la especie a reducirse y mayor es su poder oxidante. El Flúor es el oxidante más fuerte.
- Poder Reductor: Cuanto menor sea el potencial de reducción (más negativo), mayor es la tendencia a oxidarse y, por tanto, mayor es su poder reductor. El Litio es el reductor más fuerte.
- Cálculo del Potencial Estándar: Para hallar el potencial total de la pila se aplica la fórmula: Eºpila = Eºcátodo – Eºánodo.
- Espontaneidad: Una reacción redox es espontánea solo cuando su potencial es positivo (Eº > 0) y su energía libre de Gibbs es negativa (ΔG < 0). Esta relación se calcula mediante la fórmula: ΔG = -nFEº.
👀 Truco de La Llibreta: Recuerda la regla «AN-OX / CA-RED» (Ánodo-Oxidación / Cátodo-Reducción). ¡Esto nunca cambia, ya sea en una pila o en una cuba electrolítica! Lo único que cambia entre ambas son los signos de los polos
🎥 Ejercicio Resuelto en vídeo: Aquí tenéis un vídeo sobre una cuestión de la PAU de pilas electroquímicas.
5. Electrólisis: Cuando la electricidad fuerza la química
A diferencia de las pilas, la electrólisis es un proceso no espontáneo. Aquí no obtenemos corriente, sino que la consumimos: utilizamos una fuente externa (como una batería) para obligar a que ocurra una reacción química, transformando energía eléctrica en energía química.
La Cuba Electrolítica
Los dispositivos donde ocurre este proceso se llaman cubas electrolíticas (recuerda que para las pilas usamos el término «celdas galvánicas«). Sus características principales son:
- Signos de los electrodos (¡Cuidado aquí!): Es el punto donde más estudiantes fallan porque los signos se invierten respecto a las pilas.
- Ánodo (+): Polo positivo. Sigue siendo donde ocurre la oxidación.
- Cátodo (-): Polo negativo. Sigue siendo donde ocurre la reducción
- Flujo de electrones: Los electrones viajan siempre del ánodo al cátodo.
- Voltaje: Para que el proceso ocurra, debemos aplicar una diferencia de potencial mayor a la fuerza electromotriz (FEM) que tendría la pila si funcionase de forma espontánea.
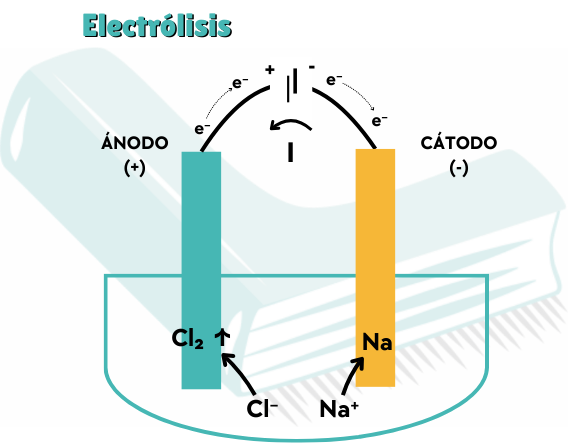
Tabla comparativa pilas galvánicas vs cubas electroquímicas:
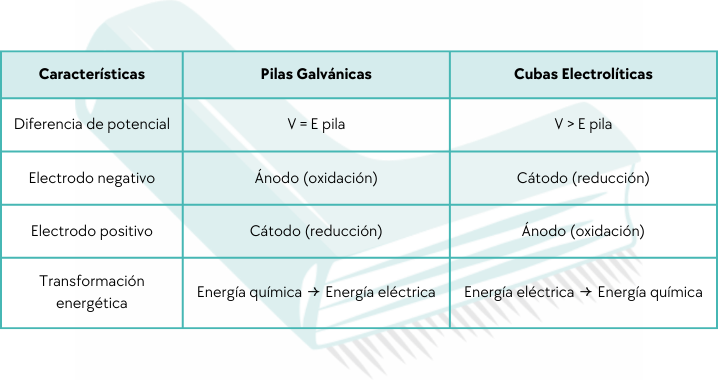
El caso crítico del NaCl: ¿Fundido o en disolución?
Este es un «fijo» en los exámenes de PAU y PCE. El resultado cambia totalmente según el estado del compuesto:
- NaCl fundido: Al no haber agua, los iones de sodio se reducen a metal en el cátodo y los de cloruro se oxidan a gas en el ánodo.
- NaCl en disolución acuosa: Aquí el agua compite con el sodio. Como el agua se reduce más fácilmente, en el cátodo obtendrás hidrógeno gaseoso (H₂) en lugar de sodio:
- Reducción (Cátodo): 2H₂O(ℓ) + 2e⁻ → H₂(g) + 2OH⁻
- Oxidación (Ánodo): 2Cl⁻ → Cl₂(g) + 2e⁻
👀 Truco de La Llibreta: Si en un problema de electrólisis en disolución te piden qué se obtiene en el cátodo, mira siempre los potenciales. La especie con el potencial de reducción más favorable (menos negativo o más positivo) será la que gane la competición y se reduzca primero
6. Las Leyes de Faraday: El cálculo de la electrólisis
Michael Faraday determinó que existe una relación directa entre la cantidad de electricidad que circula por una cuba y la masa de sustancia que se libera.
- Primera Ley: La masa de una sustancia depositada en un electrodo es proporcional a la cantidad de electricidad (Q) que atraviesa la cuba. Masa = K · Q
- Segunda Ley: Para depositar 1 mol de una sustancia, se requiere una cantidad de electricidad igual a 96.500 C (Constante de Faraday, F) multiplicada por el número de electrones (n) intercambiados en la semirreacción.
La fórmula maestra:
Para tus problemas de examen, usaremos esta expresión que combina ambas leyes:
\[
m = \frac{M \cdot Q}{n \cdot F}
\]
\[
\text{moles depositados} = \frac{Q}{F \cdot n} = \frac{I \cdot t}{96500 \cdot n}
\]
Donde
- K es la constante de proporcionalidad
- Q es la carga en coulombs (C)
- F es la constante de Faraday (aproximadamente 96,500 C/mol)
- n es el número de electrones intercambiados
🎥 Ejercicio Resuelto en vídeo: Aquí tenéis un vídeo sobre un problema de la PCE de cubas electroquímicas dispuestas en serie.
¡Vamos a por ello!
Problemas y cuestiones REDOX resueltos ve vídeo de la PAU, PCE y PAU+25
La mejor forma de preparar un examen es practicando con preguntas reales. Por eso, en La Llibreta nos esforzamos por recopilar los exámenes de convocatorias anteriores y resolverlos en vídeo, poniéndolos a disposición de toda nuestra comunidad.
🧪 PRÉPARATE EN LA LLIBRETA
En La Llibreta, ofrecemos una variedad de cursos que se adaptan a tus necesidades, tanto en formato presencial como online. Además de nuestras clases en directo, contamos con cursos online en diferido que incluyen videoclases detalladas, exámenes resueltos, resúmenes, y cuestionarios autocorregibles, entre otros recursos. También tienes la opción de comprar solo el material didáctico, sin incluir las videoclases.
Matrícula abierta 2026–2027
Reserva tu plaza para el nuevo curso
Matrícula abierta 2025-2026
¡Ultimísimas plazas para el curso anual PAU 2026!
Prepárate en la Llibreta
Prepárate con nuestroscursos híbridos. Podrás asistir de manera presencial u online. ¡Además las clases se quedan grabadas!
Compra nuestros apuntes
Tienes nuestros apuntes, esquemas, resúmens, glosarios y mucho más disponibles por 40€ y el curso de videomaterial por 190€.
Exámenes de química
Todos los exámenes de Química RESUELTOS de la EVAU, PCE, PAU+25 y PAGS
Más recursos de química
Calculadora de notas
Utiliza nuestro simulador de notas y descubre cuál es tu objetivo para que te alcance la nota de corte.
También te puede interesar
Podcast de Biología para selectividad– Episodio 8: El ciclo celular
Estrenamos podcast para Selectividad. Orgánulos y transporte a través de membrana. Hecho por nuestro equipo de súper profes.
Disoluciones y diluciones: lo que cambia, lo que se conserva y por qué te lías
Una guía clara para entender de verdad las disoluciones y las diluciones: qué es la concentración, qué cambia, qué se conserva y por qué los problemas dejan de ser difíciles cuando comprendes estas ideas básicas.
Podcast de Biología para selectividad– Episodio 7: membrana plasmática, transporte y orgánulos celulares
Estrenamos podcast para Selectividad. Orgánulos y transporte a través de membrana. Hecho por nuestro equipo de súper profes.
Cómo resolver Problemas Competenciales en Selectividad 2026 (Paso a Paso)
No es que las matemáticas sean difíciles, es que los nuevos enunciados de la PAU y la PCE están diseñados para despistarte. En este post destripamos un problema real de examen y te enseñamos la lógica que necesitas para pasar del texto a la solución sin morir en el intento.
Problemas redox de la PAU y PCE que debes saber resolver
Si te preparas para la PAU o la PCE, estos problemas de redox son imprescindibles. Descubre errores tipo y saca un 10.
Técnicas de estudio efectivas: 10 métodos que funcionan de verdad
Si sientes que estudias mucho pero avanzas poco, el problema no es el esfuerzo, sino el método. En este artículo descubrirás técnicas de estudio eficaces que se utilizan en otros países y que puedes aplicar desde hoy mismo, además de una plantilla Cornell gratuita para mejorar tus apuntes.
🎓 ¿Por qué nuestros materiales son una herramienta imprescindible?
- Diseñados por Docentes Expert@s:
Creados por profesor@s que conocen a fondo los exámenes y han seleccionado y organizado toda la información relevante para que te prepares con confianza. - Visuales, Memorables y Complejos:
Nuestros apuntes, esquemas y ejercicios están diseñados con un enfoque visual para facilitar la comprensión y la memorización, ideal tanto para estudiar en profundidad como para una rápida revisión antes del examen. - Contenido Completo y Conciso: Resúmenes claros, ejercicios resueltos y esquemas organizados en un formato fácil de manejar. Todo lo que necesitas para estudiar de manera eficiente está resumido en un solo lugar.
- Ejercicios y Exámenes Resueltos: Incluimos ejercicios interactivos, exámenes de convocatorias anteriores resueltos y organizados por bloques. Practica y refuerza lo aprendido de manera práctica y efectiva.
- Esquemas Aclaratorios: Esquemas que simplifican los conceptos más complejos, permitiéndote comprender y repasar con mayor facilidad.
Química PAU: elige tu pack y empieza hoy
Desde 20 € · acceso inmediato · material actualizado a la última convocatoria
-
Exámenes (20 €)
-
Apuntes Plus (40 €)
-
Vídeo Cursos (99 €)
-
PAU 360º (99 € + 20 €/mes)
¿Clases en directo o particulares? Haz clic aquí.
¿Te ha gustado el post? Si es así, déjanos un comentario. Durante este curso escolar, continuaremos brindándote recomendaciones y recursos para prepararte las pruebas de selectividad y PCE. ¡Ánimo en tu camino de aprendizaje! Recuerda que abordar los temas poco a poco con amor y curiosidad hará que tu viaje sea mucho más placentero.
Si te sientes perdid@, no dudes en pedir ayuda. ¡Nos apasiona lo que hacemos y estamos aquí para apoyarte en tu éxito académico!

