🧪 Cómo empezar un problema de estequiometría (sin perderte)
🌟 La guía definitiva para convertir cualquier dato en moles y resolver tus ejercicios con éxito
Muchos estudiantes se bloquean cuando ven un problema de estequiometría. No es porque no sepan química, sino porque no saben qué dato usar primero. Si te ha pasado, no te preocupes: la clave para no perderte nunca es entender que todo en química se comunica a través de una unidad común: el mol.
📺 Clase Magistral: Estequiometría desde cero
Antes de profundizar en las fórmulas, te recomiendo ver este vídeo donde te explico paso a paso cómo estructurar tu mente para resolver cualquier ejercicio:
a idea fundamental: el lenguaje de los moles
La estequiometría consiste en relacionar cantidades de sustancias que reaccionan entre sí.
Como no podemos contar átomos uno a uno, usamos los moles, que nos indican cuántas partículas
tenemos (moléculas, átomos o iones).
Para entenderlo, imagina que construyes mesas. Si 1 tablero y 4 patas producen
1 mesa, esa proporción es fija. En química ocurre lo mismo: las ecuaciones químicas nos dicen
en qué proporción reaccionan las sustancias.
Por ejemplo:
2H₂ + O₂ → 2H₂O
Esto significa que 2 moléculas de hidrógeno reaccionan con 1 de oxígeno para formar 2 de agua.
Pero como trabajamos con cantidades reales de sustancias, utilizamos moles para aplicar
estas proporciones.
🗺️ El Camino del Mol: tu mapa de resolución
Independientemente de lo que te pida el problema, casi siempre seguirás este esquema:
Datos iniciales → Moles → Relación molar → Resultado final
🧰 ¿Cómo obtener los moles según tus datos?
El primer paso para resolver un problema de estequiometría es identificar cómo convertir
los datos que te dan en moles. Estas son las formas más habituales:
1️⃣ A partir de la masa
Es la forma más común. Dividimos la masa entre la masa molar.
Fórmula: n = m / M
Ejemplo: 36 g de agua
- M(H₂O) = (2 · 1) + 16 = 18 g/mol
- n = 36 / 18 = 2 mol
2️⃣ A partir del número de partículas
Si el problema da el número de moléculas, átomos o iones, usamos el
número de Avogadro.
Nₐ = 6.022 · 10²³ partículas/mol
Fórmula: n = N / Nₐ
Ejemplo:
- 12.044 · 10²³ moléculas
- n = (12.044 · 10²³) / (6.022 · 10²³) = 2 mol
3️⃣ A partir de la concentración de una disolución
Si conocemos la concentración molar (C) y el volumen (V):
Fórmula: n = C · V
Ejemplo:
- 2 L de una disolución 0.5 M
- n = 0.5 · 2 = 1 mol
Recuerda: el volumen debe estar siempre en litros.
4️⃣ A partir del volumen de un gas
Depende de las condiciones del gas:
En condiciones normales (CN):
- 1 mol de gas ocupa 22.4 L
- n = V / 22.4
Ejemplo:
- 44.8 L de gas en CN
- n = 44.8 / 22.4 = 2 mol
En otras condiciones:
Usamos la ecuación de los gases ideales:
PV = nRT
Despejando:
n = (P · V) / (R · T)
5️⃣ A partir de densidad y volumen
Si el problema no te da la masa directamente, primero debes calcularla usando la densidad.
Paso 1: m = ρ · V
Paso 2: n = m / Mr
Ejemplo:
- 100 mL de una sustancia con densidad 0.8 g/mL
- m = 0.8 · 100 = 80 g
- n = 80 / Mr
6️⃣ A partir de la pureza de un reactivo
Si la muestra no es pura, solo la parte real del reactivo participa en la reacción.
Paso 1: masa pura
mpura = mmuestra · (pureza / 100)
Paso 2:
n = mpura / M
Ejemplo:
- 100 g al 80 % de pureza
- mpura = 100 · 0.8 = 80 g
- n = 80 / M
⚠️ Las complicaciones de los problemas de estequiometría
Una vez que sabes calcular los moles, muchos problemas añaden información extra
que complica el cálculo.
Pureza
Si un reactivo tiene una pureza del 80 %, significa que el 20 % son impurezas
que no reaccionan. Siempre debes calcular primero la masa pura.
Reactivo limitante (RL)
Es el reactivo que se consume primero y detiene la reacción.
Ejemplo: si tienes 3 tableros y 10 patas para construir mesas, solo puedes hacer
2 mesas porque las patas se acaban antes.
El reactivo que permite formar menos producto es el reactivo limitante.
Rendimiento
La estequiometría calcula la cantidad teórica de producto,
pero en la práctica siempre se obtiene menos.
El rendimiento indica qué porcentaje del producto teórico se obtiene realmente.
Rendimiento (%) = (cantidad real / cantidad teórica) · 100
Infografía para entender la estequiometría
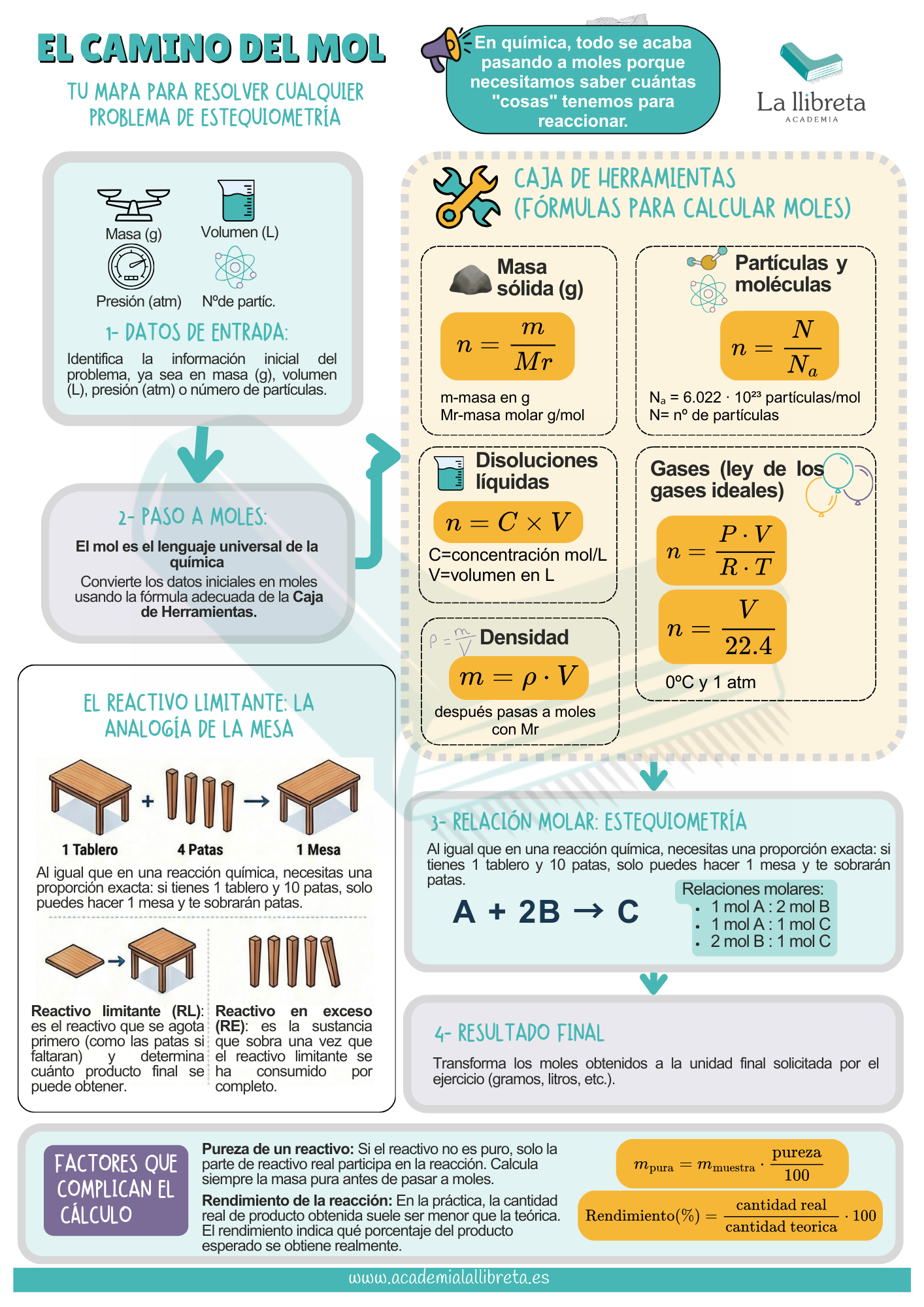
Para que siempre tengas a mano este «mapa de carreteras», he preparado una infografía de estequiometría que resume los puntos clave de la lección. En el estudio de la química, contar con un recurso visual es la mejor forma de evitar el bloqueo cuando los datos parecen complicados.
Esta guía visual te ayudará a resolver problemas de estequiometría paso a paso, mostrando claramente el camino universal: desde los datos iniciales hasta el resultado final, pasando siempre por el mol. En ella encontrarás todas las fórmulas esenciales para calcular moles a partir de la masa, gases o disoluciones, facilitando el trabajo con conceptos críticos como el reactivo limitante y la pureza de las muestras.
¡Guarda esta imagen para tus repasos de Bachillerato y PAU/PCE! Es la herramienta definitiva para entender cómo empezar un problema de química sin perderte.
🧠 ¿Realmente has entendido el «Camino del Mol»? ¡Ponte a prueba!
Antes de lanzarte a resolver problemas complejos, es fundamental que compruebes si los cimientos están claros. ¿Sabrías responder qué dato usar primero en un examen? ¿Tienes clara la diferencia entre el reactivo limitante y el reactivo en exceso? ¿O cómo afecta la pureza de una muestra al cálculo de los moles?
No te quedes con la duda. Hemos preparado unos cuestionarios rápidos para que valides tu nivel de comprensión de forma inmediata. Es la mejor manera de detectar si hay algún concepto que todavía se te escapa antes de pasar a la práctica real.
👉 Haz clic aquí para realizar el Test Online de Estequiometría
Una vez que superes el test y demuestres que dominas la relación molar, estarás totalmente listo para los ejercicios que vienen a continuación. ¡A por ello!
Matrícula abierta 2025-2026
Últimas plazas para nuestro curso anual
Prepárate en la Llibreta
Prepárate con nuestroscursos híbridos. Podrás asistir de manera presencial u online. ¡Además las clases se quedan grabadas!
Compra nuestros apuntes
Tienes nuestros apuntes, esquemas, resúmens, glosarios y mucho más disponibles desde 20€.
Exámenes de química
Todos los exámenes de Química RESUELTOS de la EVAU, PCE, PAU+25 y PAGS
Más recursos de química
Calculadora de notas
Utiliza nuestro simulador de notas y descubre cuál es tu objetivo para que te alcance la nota de corte.
También te puede interesar
Ejercicios de Estequiometría: Test Online para Entender Moles, RL y Disoluciones
🧪 Ejercicios de Estequiometría para Pensar (y Entender de Verdad la Química) 🌟 Practica la estequiometría con ejercicios autocorregibles, explicaciones claras y tests diseñados para que aprendas razonandoEste post no es solo teoría: es un campo de prácticas de...
Ajustar reacciones químicas nunca había sido tan fácil
Aprende a ajustar reacciones químicas sin miedo Aprende con explicaciones claras y ejercicios interactivos pensados para ayudarte de verdadHola, Hoy queremos ayudaros a dominar el ajuste de reacciones químicas. Sabemos que para muchos/as estudiantes que empiezan con...
Problemas de ácido base en PAU y PCE que tienes que saber resolver
Si te preparas para la PAU o la PCE, estos problemas de ácido base son imprescindibles. Descubre errores tipo y saca un 10.
Ácido-Base para PAU y PCE: Resumen, Trucos y Problemas Resueltos
Domina el equilibrio químico PAU PCE con nuestros consejos y trucos para resolver problemas complejos y comunes en Selectividad.
Equilibrio Químico para PAU y PCE: Resumen, Trucos y Problemas Resueltos
Domina el equilibrio químico PAU PCE con nuestros consejos y trucos para resolver problemas complejos y comunes en Selectividad.
Problemas de equilibrio químico en PAU y PCE que debes saber resolver
Si te preparas para la PAU o la PCE, estos problemas de equilibrio químico son imprescindibles. Descubre errores tipo y saca un 10.
Tabla de Iones Comunes y Trucos para Disociar Compuestos Químicos en Selectividad
Descubre la tabla de iones comunes y cómo se disociación los compuestos químicos para resolver ejercicios de selectividad.
⚗️Cinética Química para Selectividad y PCE – Resumen y Ejercicios Resueltos
Te contamos los aspectos claves del tema de estructura de la materia para el examen de selectividad de la Comunidad Valenciana y la PCE.
⚗️Primer Principio de la Termodinámica explicado: Termoquímica y recursos clave
Descubre el Primer Principio de la Termodinámica de forma clara y sencilla. Aprende sobre calor, trabajo, energía interna y más con ejemplos prácticos y recursos únicos.
Cómo aprobar un examen Tipo Test en las PCE Selectividad
¿Estás preparando las PCE y te enfrentas a exámenes tipo test? En este artículo encontrarás estrategias efectivas, consejos clave y recursos gratuitos para que practiques al máximo. Además, te ofrecemos cursos y materiales exclusivos que harán que tu preparación sea más completa. ¡Inscríbete y supera las PCE con éxito!
🎓 ¿Por qué nuestros materiales son una herramienta imprescindible?
- Diseñados por Docentes Expert@s:
Creados por profesor@s que conocen a fondo los exámenes y han seleccionado y organizado toda la información relevante para que te prepares con confianza. - Visuales, Memorables y Complejos:
Nuestros apuntes, esquemas y ejercicios están diseñados con un enfoque visual para facilitar la comprensión y la memorización, ideal tanto para estudiar en profundidad como para una rápida revisión antes del examen. - Contenido Completo y Conciso: Resúmenes claros, ejercicios resueltos y esquemas organizados en un formato fácil de manejar. Todo lo que necesitas para estudiar de manera eficiente está resumido en un solo lugar.
- Ejercicios y Exámenes Resueltos: Incluimos ejercicios interactivos, exámenes de convocatorias anteriores resueltos y organizados por bloques. Practica y refuerza lo aprendido de manera práctica y efectiva.
- Esquemas Aclaratorios: Esquemas que simplifican los conceptos más complejos, permitiéndote comprender y repasar con mayor facilidad.
Química PAU: elige tu pack y empieza hoy
Desde 20 € · acceso inmediato · material actualizado a la última convocatoria
-
Exámenes (20 €)
-
Apuntes Plus (40 €)
-
Vídeo Cursos (99 €)
-
PAU 360º (99 € + 20 €/mes)
¿Clases en directo o particulares? Haz clic aquí.

